泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2015-07-20 转至微博:
|
医药网7月18日讯 为全面反映2014年我国药品不良反应监测情况,促进临床合理用药,保障公众用药安全,依据《药品不良反应报告和监测管理办法》,国家食品药品监督管理总局组织编撰国家药品不良反应监测年度报告(2014年)。
一、不良反应监测工作情况
2014年,全国药品不良反应监测工作取得新进展:
监测网络覆盖面进一步拓宽,报告数量进一步增长。2014年,全国已有24万余个医疗机构、药品生产经营企业注册为药品不良反应监测网络用户,并通过该网络报送药品不良反应报告,其中医疗机构仍是报告的主要来源。全国94.4%的县有药品不良反应报告,全国每百万人口平均报告数量达到991份,较2013年有一定增长,表明我国发现和收集药品不良反应信息的能力进一步增强。
深入开展数据评价分析,提高风险信号挖掘能力。2014年通过日监测、周汇总、季度分析等方法加强对国家药品不良反应监测数据库数据的评价分析,深入挖掘药品风险信号,对阿德福韦酯、胞磷胆碱钠、苯溴马隆等近50个(类)品种进行了安全性评价,并采取了相应的风险管理和沟通措施。
建立全国联动工作机制,发挥监测预警能力。进一步完善药品聚集性事件预警平台,建立预警信息全国共享、事发地和生产企业所在地食品药品监管部门协同调查处置联动工作机制,保证药品质量风险的早发现、早评价、早控制。全年重点分析评价137条预警信息,及时发现并处置了湖北同济奔达鄂北制药有限公司核黄素磷酸钠注射液、安徽联谊药业股份有限公司胞磷胆碱钠注射液、吉林省集安益盛药业有限公司生脉注射液等多起因药品质量问题引发的不良事件,有效保障公众用药安全。
推动企业落实责任,提高风险管理水平。2014年积极推进药品定期安全性更新报告工作,加强对企业撰写报告质量的培训,严格开展对报告的审核,促进企业落实风险管理意识;完善药品不良反应数据共享平台,及时将监测数据和风险信号反馈药品生产企业,指导企业进行数据分析评价与利用,督促企业落实安全风险主体责任,持续提高药品安全保障水平。
二、药品不良反应/事件报告情况
(一)报告总体情况
1. 年度及月度药品不良反应/事件报告情况
2014年全国药品不良反应监测网络收到《药品不良反应/事件报告表》132.8万份,较2013年增长了0.8%。其中新的和严重药品不良反应/事件报告34.1万份,占同期报告总数的25.7%。1999年至2014年,全国药品不良反应监测网络累计收到《药品不良反应/事件报告表》近790万份。
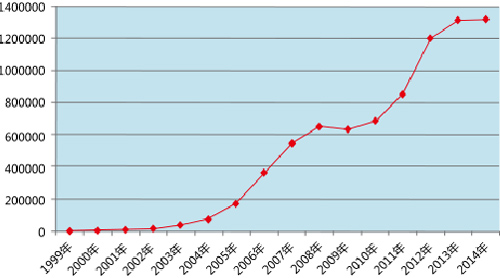 图1 1999-2014年全国药品不良反应/事件报告数量增长趋势
2014年月度病例报告数量在整体趋势上与2013年基本相同,报告数量主要集中在10-12月,其中11月是报告高峰,但月度报告数量差距逐渐缩小,集中上报现象逐步缓解。
 图2 2013-2014年药品不良反应/事件月度报告数变化趋势
2.新的和严重药品不良反应/事件报告情况
新的和严重药品不良反应/事件报告是药品不良反应监测的重点,新的和严重报告比例,尤其是严重报告比例是衡量总体报告质量和可利用性的重要指标之一。2014年全国药品不良反应监测网络收到新的和严重药品不良反应/事件报告341,300余份,与2013年比增长了17.0%;新的和严重报告数量占同期报告总数的 25.7%,与2013年比增加了3.6个百分点。
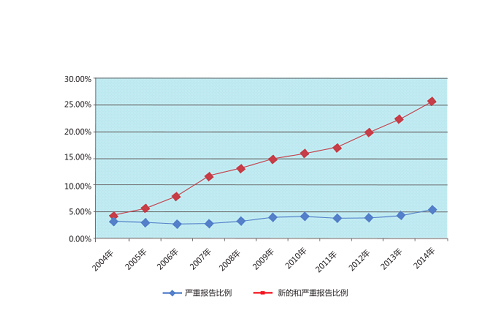 图3 2004-2014 年新的和严重以及严重药品不良反应/事件报告比例
3.每百万人口平均病例报告情况
每百万人口平均病例报告数量是衡量一个国家药品不良反应监测工作水平的重要指标之一。2014年我国每百万人口平均病例报告数为991份,与2013年相比增加了0.8个百分点。
4.药品不良反应/事件县级报告比例* ?
药品不良反应/事件县级报告比例是衡量我国药品不良反应监测工作均衡发展及覆盖程度的重要指标之一。2014年全国药品不良反应/事件县级报告比例为94.4%,与 2013年相比增长了0.6个百分点。
5.药品不良反应/事件报告来源
按报告来源统计,医疗机构的报告占82.2%、药品经营企业的报告占16.0%、药品生产企业的报告占1.4%、个人及其他来源的报告占0.4%。与2013年相比,医疗机构报告增长明显,药品生产企业报告比例与既往持平,经营企业报告比例继续下降。
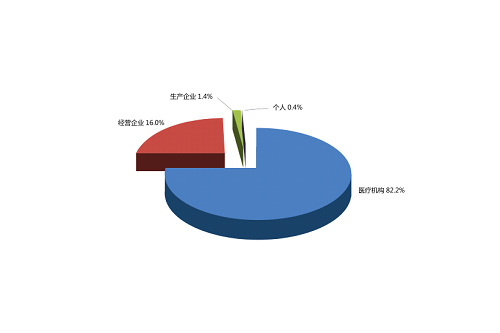 图4 2014年药品不良反应/事件报告来源分布
6.报告人职业
按照报告人职业统计,医生报告占53.8%;药师报告占27.3%;护士报告占14.0%,其他报告占4.9%。与2013年的报告人职业构成情况基本相同。
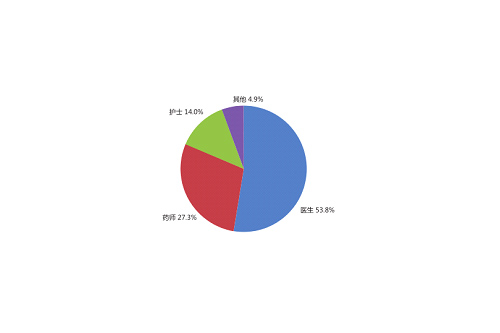 图5 报告人职业构成
7.药品不良反应/事件报告涉及患者情况
按报告涉及患者年龄统计,14岁以下儿童患者的报告占10.5%,与2013年基本一致,65岁以上老年人的报告占19.9%,较2013年升高了2.1个百分点。
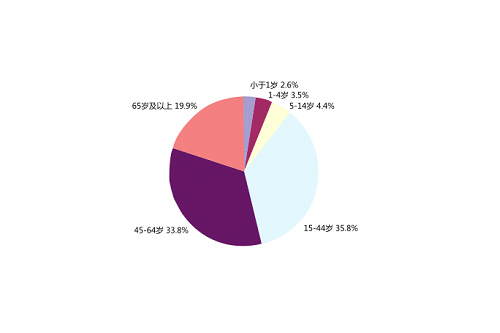 图6 2014年药品不良反应/事件报告年龄分布
8.药品不良反应/事件报告涉及药品情况
按怀疑药品类别统计,化学药占81.2%、中药占17.3%、生物制品占1.5%。抗感染药报告数量仍居首位,占化学药的46.2%,较2013年降低了1.4个百分点,报告比例已连续5年呈下降趋势。心血管系统用药占化学药的10.2%,较2013年上升了0.2个百分点,且连续5年呈上升趋势。
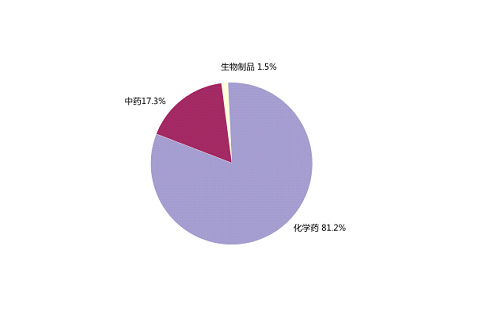 图7 2014年药品不良反应/事件报告涉及药品类别分布
按药品剂型统计,2014年药品不良反应/事件报告涉及的药品剂型分布中,注射剂占60.9%、口服制剂占35.2%、其他制剂占3.9%。注射剂所占比例较2013年升高了2.2个百分点,口服制剂比例降低了2.1个百分点。
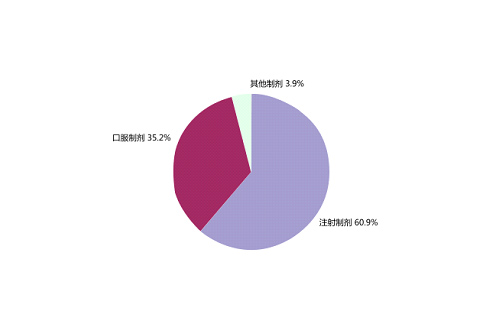 图8 2014年药品不良反应/事件报告涉及药品剂型分布
按照药品给药途径统计,2014年药品不良反应/事件报告涉及的药品给药途径分布中,静脉注射给药占57.8%,其他注射给药占3.0%,口服给药占36.2%,其他给药途径占3.0%,与2013年相比,静脉注射给药的比例上升2.1个百分点,口服给药比例降低2.2个百分点。
9.累及系统及主要不良反应表现
2014年报告的药品不良反应/事件中,累及系统排名前三位的为皮肤及其附件损害(占27.8%)、胃肠系统损害(占26.3%)和全身性损害(占12.2%),前三位之和为 66.3%。化学药、中成药累及系统前三位排序与总体一致,但生物制品累及系统前三位与总体有所不同,依次是皮肤及其附件损害、全身性损害和呼吸系统损害。
注射剂型累及系统前三位与总体报告一致,分别是皮肤及其附件损害(占32.9%)、胃肠系统损害(占18.9%)、全身性损害(占14.6%),口服制剂累及系统前三位为胃肠系统损害(占41.6%)、皮肤及其附件损害(占17.0%)、中枢及外周神经系统损害(12.2%)。与2013年基本一致。
化学药注射剂的不良反应表现多为皮疹、瘙痒、恶心、呕吐、胸闷、过敏反应、头晕、心悸、寒战、发热等,化学药口服制剂的不良反应表现多为恶心、皮疹、呕吐、头晕、瘙痒、头痛、腹泻、腹痛、口干、咳嗽等;中药注射剂的不良反应表现多为皮疹、瘙痒、胸闷、恶心、心悸、寒战、过敏反应、头晕、呕吐、呼吸困难等,中成药口服制剂的不良反应表现多为恶心、腹泻、皮疹、呕吐、腹痛、瘙痒、头晕、胃不适、口干、头痛等。
10.药品不良反应/事件报告总体情况分析
2014年药品不良反应/事件报告总体情况与 2013年相比未见显著变化。在患者年龄分布中,老年患者不良反应报告比例依然呈现小幅增高态势。在剂型和给药途径分布中,注射剂和静脉给药的比例依然呈现上升趋势,提示应加强相关宣传、教育工作。在化学药总体排名和按剂型分布的排名中,心血管系统用药所占比例均有所增加。随着我国居民生活水平的提高,心血管疾病的发病率在逐年升高,心血管系统用药尤其是口服制剂使用越来越广泛,应进一步加强心血管系统用药监测与评价。
关键词:
|