泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2016-07-25 转至微博:
|
医药网7月25日讯 近日,CDE给了药企一个利好。
7月21日,国家局药品审评中心出台了一极为简练的《“首仿”品种实行优先审评评定的基本原则》。原则总计249字。从发布意义上而言,该文件更像部门工作计划调整的告知函。CDE在该文件从药品申报上提出了部门内部的“首仿药”的定义,并将首仿药的申报注册纳入优先范畴。这将大大提速首仿药物的上市进程。
首仿药需同时满足以下条件:
(一) 同品种仅有一家进口上市;
(二) 待审评同品种中,按药品审评中心承办日期先后顺序属于第一家的;
(三) 已经超出法定审评期限。
首仿药以前无官方定义
“首仿”概念源于美国首仿药的概念,《药品价格竞争和专利期恢复法》(Hatch-Waxman修正案)规定,在“专利无效或者批准正在申请的药物不会侵犯专利”的情况下,第一个仿制申请者将拥有180天的市场专卖权,在此期间,FDA不再批准相同的ANDA(新药上市申请)。
“首仿药物”在我国优待地位并不明显,根据2016年3月国家局发布的《化学药品注册分类改革工作方案》,首仿药物并不存在以上保护期。“首仿药物”价值更多体现药品招标中,在双信封制度的技术评分的加分。
2005年发改委在《药品价格管理办法》中提出了首仿概念,定义为国内首先仿制生产并上市销售的药物。在2006年国家发改委发布的《药品定价办法》(征求意见稿)一文中,官方提出单独定价药品的概念,指出“符合下列条件之一的同种仿制类药品,经专家论证后,允许在统一定价基础上适当上浮价格:……国内首先仿制生产并上市销售的”。根据物价部门组织的单独定价认定流程,由专家论证确定企业所申报的产品是否为首仿药,从而获得单独定价资格。
而后续一些省份招标文件中,将“首仿药物”、“单独定价药物”列为较高质量层次,实行单独竞价组,或进行一定的溢价处理。
由于部门间数据未有效对接,且首仿药的定义在各省招标文件的更新,内涵不断延伸,是否为首仿药在我国没有一个官方的界定标准。该资格认定主要以各省招标办根据企业主张及提交的材料审核,在文件公示无质疑后定义为首仿药物。
但各省招标规则认定的首仿药物,普遍要求:首家仿照国外专利技术生产的药品,以国家食品药品监督管理局批准文号批准时间,结合质量标准起草证明为依据,同时持有新药证书的国产药品等。
首仿药规则宽泛,利好
而本次CDE公布的“首仿药物”优先评审清单,所列出产品主要为6类注册(即国内已有上市的仿制),远较原来各省规则宽泛。
从招标的角度而言,如果一家进口和一家国内首仿厂家同时共存,进口厂家以过期原研单列,国内厂家质量层次分组中属于独家,此时国内厂家更希望通过注册获得更长的独占期而非招标意义上的"首仿"。
唯有同产品多家的"首家"厂家更希望从获批时间差中获得价格优势和中标分组单一货源供应。随着一致性评价的法规的推进,药品招标的质量分层更加关注的是否通过一致性评价。
结语:首仿由CDE认定,招标利好
CDE对首仿药的定义中有一个重要的条件是:已经超出法定审评期限。这个定义表明只有超过注册时间的才能补偿待遇,这意味如果申报正常按时获批的首仿药物并没有加快。因此这个今天引起了较多规则的政策,可能只是短期政策。而对一些有多家生产的药品而言,在药品的资质认定中,也许能通过CDE的这个定义获得一些招标优势。
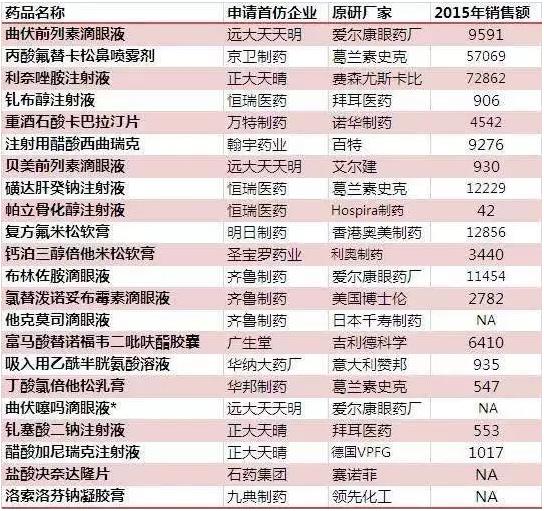
附:首仿药优先审评名单及2015年市场销售规模(万元)
关键词:
|