泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2017-04-18 转至微博:
|
医药网4月13日讯 11日,江西赣州市药监局印发《2017年赣州市药品生产监管工作要点》,其中,江西青峰药业有限公司、江西润泽药业有限公司等20家药企的品种被列为重点监管品种。
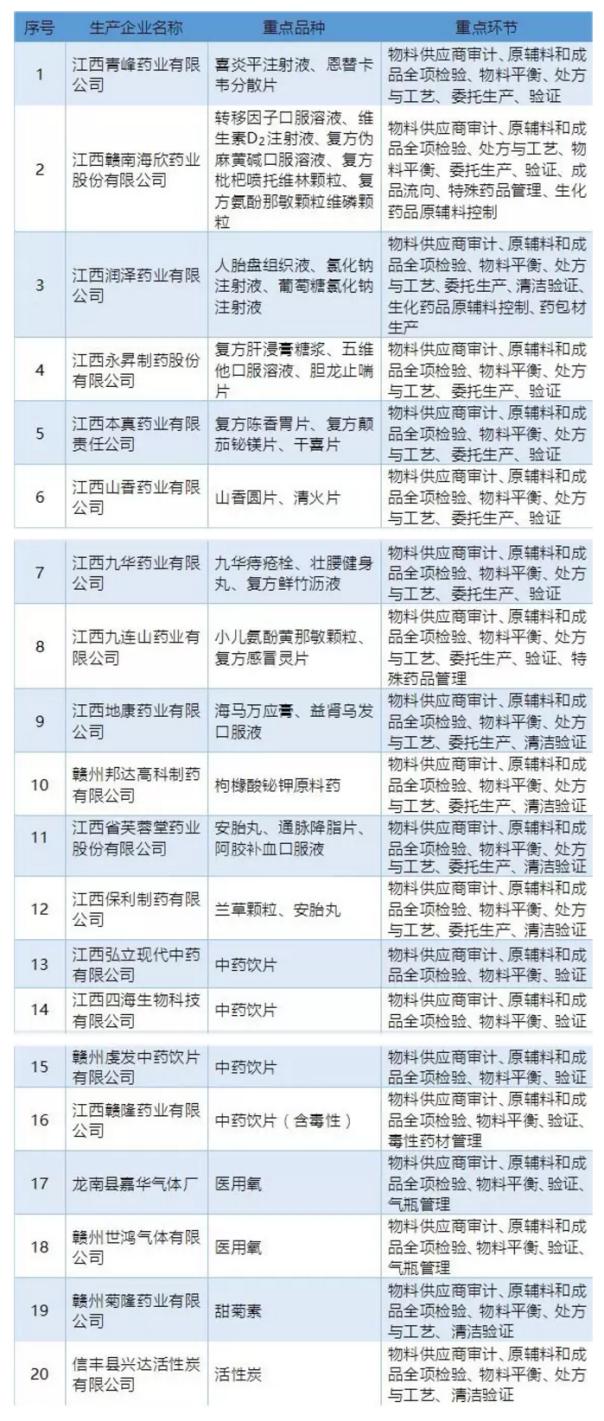 附:
2017年赣州市药品生产监管工作要点
2017年,全市药品生产监管工作必须严格按照全省工作要点,结合本市监管实际,坚持以问题为导向,围绕“确保药品质量安全,防范系统性风险发生”中心,重拳整治药品生产领域的突出问题,严厉打击药品生产领域的各种违法违规行为,确保药品生产质量安全。
一、开展专项整治,消除药品生产质量安全隐患
(一)开展中药饮片生产专项整治。市局将组织稽查、药检及相关县(市、区)局人员,按照《关于开展中药饮片生产企业专项检查的紧急通知》(赣食药监药化生产〔2017〕8号)的要求,集中开展中药饮片生产专项整治,依法严肃处理虚开票据,染色增重,掺杂使假,外购饮片贴牌分装,出租出借证照,违规生产毒性中药饮片等违法违规行为,检查结果于2017年4月5日前报省局。
(二)开展多组分生化药生产专项整治。各相关县(市、区)局要组织对辖区内多组分生化药品(P-转移因子、人胎盘组织液等)进行专项检查,重点检查多组分生化药品原辅料控制情况,严厉打击外购他人提取后废料进行生产的严重违法行为。
(三)开展用贵细和胶类产品投料专项整治。重点检查企业是否存在贵细药材(如牛黄等)不投料或少投料;使用假劣药材代替贵细药材投料等情况,如骡子皮、马皮代替驴皮,使用猪胆、牛胆代替蛇胆和熊胆投料等问题。
(四)开展中药提取物生产专项整治。要对辖区内生产和使用中药提取物的企业逐一排查,认真核算企业的提取能力与产能,采取延伸检查等方式,严厉打击违法生产提取物、违法购用和不按规定备案提取物等行为。对异地设立或共用提取车间、使用备案的提取物等情形,必须全覆盖开展延伸检查。
(五)开展药品委托生产专项整治。重点检查是否有非法委托或非法接受委托生产药品的行为,委托双方是否切实履行了各自的义务,所生产的产品质量是否稳定。
(六)开展注射剂等高风险产品专项整治。重点检查企业对热原、细菌内毒素、无菌检查等环节的控制是否符合要求,是否严格履行了对产品稳定性考察的相关要求。
(七)开展生产专项检查。重点检查高风险药包材生产企业是否按要求对生产所用原料严格把关,是否按批准的配方、工艺、规格组织生产,生产记录是否完整,厂房净化条件是否达到要求;是否具有国家食品药品监督管理局核发的药包材注册证,购进渠道是否合法、资质证明是否齐全。
(八)开展药品标准执行情况专项检查。重点检查企业药品生产和检验是否严格按照法定标准执行;产品检验是否按照标准进行了全项检验。
对上述八类问题,各相关县(市、区)局要高度重视,结合各自实际,梳理涉及产品清单,找准问题根源,突出整治重点,采取集中行动,重点查处和打击生产过程中擅自改变工艺、非法添加、数据造假等违法行为。各相关县(市、区)局应于2017年10月25日前将专项检查情况报市局药化生产监管科。
二、加强重点企业、重点品种和重点环节的监管
(一)各相关县(市、区)局要开展对取得《药品生产许可证》的药品生产企业、已备案的提取物生产企业、医疗机构制剂室全覆盖监督检查,不留监管盲区和死角。
(二)加强对重点企业监管。重点加强对生产注射剂、生化药品、接受境外委托加工或出口药品、不良反应多、抽检不合格等的企业,被发布风险警示药品的企业,近三年新开办药品生产企业,长期处于停产或半停产企业、近三年被收回药品GMP证书的企业的监管。各相关县(市、区)局对重点监管企业监督检查频次每半年不得少于1次,市局将对重点监管企业进行抽查。
(三)加强对重点品种监管。重点对基本药物品种、原料药紧缺品种的制剂、价格倒挂品种、特殊药品(含特殊药品的复方制剂)、近年来不合格批次较多品种、药品不良反应较多品种、近三年新上市品种、使用鲜竹沥为原料的品种(见上表)的监管。
(四)加强对重点环节监管。重点加强对物料供应商审计、原和成品全项检验、物料平衡、不合格品处置、委托生产、清洁验证等(见上表)监管。
(五)加强药品生产安全监管。监督企业加强对危险化学品及特殊药品使用设施、设备、安全附件的安全检查,加强对产尘、高温、高压、易燃、易爆等重点车间、重点部位的安全监控,及泄露检测报警、通风、防火防爆设施设备维护及运行的检查,加强对麻醉药品、精神药品、毒性药材(药品)、易制毒化学品、菌毒种和危险化学品的管理。各相关县(市、区)局在日常监督检查中强化安全生产的监管,认真履行“一岗双责”,确保企业不出安全生产事故。
(六)加强数据可靠性检查。要将数据可靠性作为检查重点内容,对企业生产、检验全过程的数据不可溯源、不真实的情况要严肃处理。
(七)协助省局督促和指导企业对相关产品开展仿制药质量和疗效一致性评价工作。
三、建立和完善生产监管机制
(一)建立药品安全风险分析研判制度。各相关县(市、区)局要建立药品安全风险分析研判制度,针对本地区行业特点和问题线索,主动排查问题,消除隐患。加强信息交流和共享,形成风险发现、风险评估、风险处置和风险交流工作机制。对可能存在的系统性风险,要及时向上级部门报告,以便采取统一行动消除风险,严守药品安全的底线。
(二)建立联合检查制度。市局将建立药品生产监管、药品稽查、药品检验联合检查制度,统一调配本辖区药品生产监管、药品稽查、药品检验人员,组成联合检查组开展对药品生产监督检查,各相关县(市、区)局要积极配合,并结合各地实际,建立相应的检查制度。
(三)建立健全严格的责任落实机制。各相关县(市、区)局要有严明的工作纪律,明确工作责任,确保政令畅通,不打折扣。市局将开展考核评议工作,严格实施药品监督管理责任制和责任追究制。
四、加强对不合格产品、风险警示品种的处置和隐患排查
(一)依法严肃处理生产不合格产品的企业。对每一批次不合格产品要追根溯源,上查源头、下查终端,依法严肃处理生产不合格产品的相关企业,并公开处理结果。监督企业迅速暂控、召回和销毁问题产品。
(二)通过药品检验提示信息发现药品安全隐患。各相关县(市、区)局要督促企业对不合格产品和风险警示品种深入分析,排查产生的原因,并举一反三,从中找出企业在质量保障体系、原辅料、处方、生产工艺、包装储运等方面可能存在的问题,并监督企业切实整改,督促企业完善和提高原辅料和成品质量内控标准,消除安全隐患。
五、加强特殊药品监管工作
(一)建立并完善特殊药品监管机制。开展对药品类易制毒化学品及其制剂、麻醉药品和第一类精神药品批发企业专项检查,完善特殊药品监管巡查制度。积极配合全市禁毒工作部署,确保特殊药品不发生流弊现象。
(二)落实特药日常监管责任。各相关县(市、区)局对特殊药品生产制剂企业和麻醉药品、第一类精神药品区域性批发企业以及药品类易制毒化学品定点批发企业的监督检查,每季度不少于1次;对其他特殊药品经营企业和使用特殊药品为原料的生产企业、使用放射性药品的医疗机构的监督检查,每半年不少于1次。
(三)认真组织开展第二类精神药品专项整治。对第二类精神药品制剂特别是含可待因复方口服液体制剂的经营企业及相关品种的专项检查,检查覆盖率达100%,重点核实所经营品种的销售流向,要对流向的下游单位(企业)抽查20%以上(不少于5家单位)。一旦发现问题,立即依法处理,逐级上报,并通报公安机关。
六、配合做好药品GMP认证工作
各相关县(市、区)局要配合好省药品认证中心的工作,积极参加全省的认证现场检查,并严格按新修订药品GMP标准执行。同时,加强药品GMP检查员队伍建设,积极参加省药品认证中心组织的各类培训,在学习中不断提高监管水平。
七、加强药品不良反应监测工作
(一)加强药品不良反应制度建设。市药品不良反应监测中心要严格按照省局制定的《药品不良反应现场处置管理办法》的现场处置原则、处置程序、药品抽样等规定进行现场处置,进一步规范药品不良反应现场处置工作程序。
(二)加强药品不良反应监测数据分析工作。市药品不良反应监测中心要对聚集性药品不良信号背后隐含的可能与药品质量有关的信息进行分析,并将信息及时通报相关药品监管部门,为及时快速处置赢得主动和时间。
(三)加强药品生产企业不良反应共享数据的核实与分析评价工作。各相关县(市、区)局和市药品不良反应监测中心要督促药品生产企业每月按时完成数据的下载、核对、分析、评价,每半年提交不良反应数据分析报告,提取风险信号,依据风险信号及时采取风险管理措施。
八、加强药品生产监管信息报送工作
各相关县(市、区)局要根据省局制定的药品生产监管工作要点,结合本辖区监管工作实际,按照本市药品生产监管工作要点开展药品生产质量安全监管,并按规定的要求及时上报各项信息。
关键词:
|