泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2018-05-27 转至微博:
|
医药网5月22日讯 制药领域几乎每年都有数十个品牌药失去专利保护,廉价仿制药因而迎来市场机会。如今,生物类似药的出现似乎带来了一些不同以往的市场现象。过去,专利过期会给原研药企带来仿制药竞争及市场冲击。随着生物技术的发展,专利的损失并不一定会为仿制药企敞开大门。
罗氏(Roche)的重磅药Rituxan是今年面临专利悬崖的药物中销售额最高的产品,这迫使罗氏从新药中寻求增长机会。其次是安进(Amgen)的白细胞生成刺激因子药物Neulasta,今年可能会面临来自迈兰(Mylan)的首只生物类似药的竞争。事实上,Neulasta的专利早在2015年就已到期。
还有不少类似的例子,原研药专利期满后,仿制药或生物类似药未立刻上市。FiercePharma近期汇总了美国2018年将失去专利保护,或过去几年已失去专利保护但尚未受到仿制药或生物类似药威胁的畅销药物。
其中,2017年销售额排名前十的产品均为“重磅炸弹”,其在美国市场的销售总额接近230亿美元。
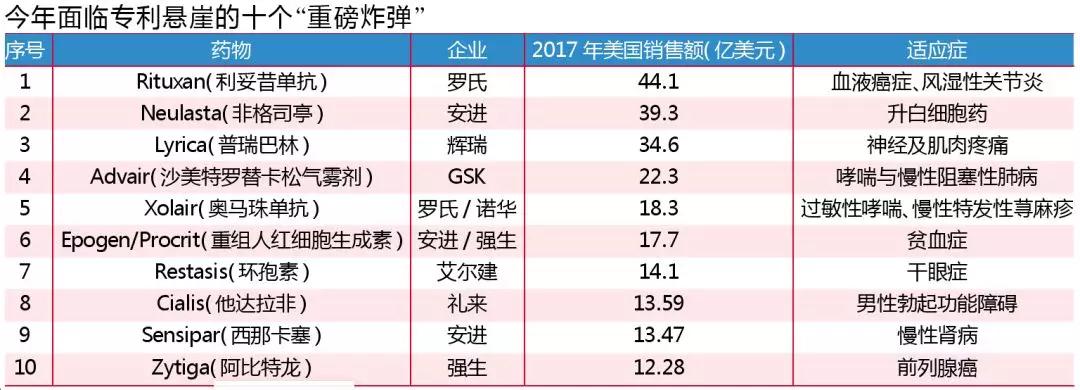 1、Rituxan:英国八成市场被蚕食
[生物类似药预计上市时间(美国市场,下同)] 不确定
在欧洲市场遭到生物类似药蚕食之后,罗氏最畅销的生物药Rituxan今年在美国市场或许也将迎来生物类似药的竞争。
Rituxan于1997年在美国首次获批。该药目前可治疗特定的患有滤泡性淋巴瘤、弥漫性大b细胞淋巴瘤和慢性淋巴细胞性白血病的患者。2017年,该药在美国创造了44.1亿美元的销售额。包括辉瑞(Pfizer)、迈兰(Mylan)和安进(Amgen)在内的许多公司都在研发Rituxan的生物类似药,山德士(Sandoz)和梯瓦(Teva)已将生物类似药申请提交给FDA。
与欧洲相比,复杂的专利保护和诉讼致使生物类似药在美国市场发展较慢。2017年,欧洲市场生物类似药已减少了Rituxan 11%的销售额。据报道,赛尔群(Celltrion)的生物类似药2017年在英国上市,现已占据该国80%的市场份额。
此前分析人士预计Rituxan的生物类似药将于今年在美国上市,但近日山德士收到FDA的完整回复函,又为产品上市增加变数。
Rituxan并不是罗氏近期唯一面临市场竞争的产品。曲妥珠单抗(Herceptin)可能在明年面临生物类似药竞争,贝伐单抗(Avastin)则将到2020年。
这3只药物在2017年带来的总销售额超过210亿美元,今后罗氏不得不依靠新药来维持增长,例如Ocrevus和Hemlibra,其在2017年分别被批准用于治疗多发性硬化症和血友病。
2、Neulasta:今年两个竞争者来袭
[生物类似药预计上市时间] 2018年年中
在2015年专利到期后,安进的明星药Neulasta今年将面临第一只生物类似药的竞争。今年1月在美国旧金山举行的J.P摩根医疗投资大会上,迈兰总裁Rajiv Malik透露,该公司将在今年中期推出Neulasta的生物类似药。
Neulasta于2002年首次获批,去年该药在美国市场的销售收入达到39.3亿美元。
山德士也将推出Neulasta的生物类似药,收到FDA的完整回复函后,其计划在2019年重新提交申请。据瑞穗银行(Mizuho)分析师介绍,Coherus、Pfenex和辉瑞也有相关生物类似药研发项目正在开展。
Coherus在2017年第四季度财报中透露,今年下半年将在美国上市Neulasta生物类似药。近期,安进对Coherus的专利诉讼失败。药物管理和分析公司Optum认为,该药将在2018年第四季度或更晚些时候进入市场。
3、Lyrica:巨额广告支出欲留住客户
[专利到期时间] 2018年12月30日
辉瑞的Lyrica已获得了不俗的销售成绩,但其在美国的市场独占权将要终结,除非能获取药专营延期资格,该药才有可能将独家销售延长至明年。
该药在2004年首次获批,去年是辉瑞销售额最高的,在美国市场创造了34.6亿美元的销售额。
Lyrica是近几个月辉瑞实施提价政策的药物之一。随着专利期限临近,辉瑞在面向消费者的广告上也投入了大量资金,2017年这部分支出在制药巨头中居于第二高位,仅次于艾伯维的抗风湿性关节炎重磅药阿达木单抗(Humira)的相关广告费用。2017年,Lyrica仅在电视渠道就投放了2.16亿美元的广告。
目前,迈兰、梯瓦和山德士的仿制药已获得FDA的暂时性批准。
Lyrica CR于去年10月获批,其将用于带状疱疹或糖尿病周围神经病变引起的疼痛,与Lyrica原版所治疗的纤维肌疼痛有所区别。Lyrica CR每日只需服用一次,而Lyrica是每天两到三次。
4、Advair:复杂装置挡住仿制药
[仿制药预计上市时间] 不确定
多年来,葛兰素史克(GlaxoSmithKline)一直在为其最畅销的Advair的仿制药竞争做足准备。
事实上,该药早在2010年就已失去专利保护。但由于Diskus吸入器技术难以复制,此前仿制药开发者多数遭遇失败。2013年9月,FDA发布了该药的仿制药研发指南。尽管如此,3家仿制药企——迈兰、Hikma-Vectura和山德士的申请还是遭到FDA拒绝,目前还不清楚其何时能通过审批。
2017年5月,迈兰的仿制药申请第一个遭受拒绝,尽管该公司自信满满;Hikma与Vectura联合研发的仿制产品同样被拒,这两家公司随后向FDA提出疑议。此后该项目继续回归临床试验,并提出额外临床终点研究的申请,预计最快获批也要到2020年;今年2月,FDA同样驳回了山德士的申请,发出了完整回复函,该产品年内是否有机会上市还难以确定。
尽管Advair的美国销售额已因支付方降价压力和折扣而趋于下降,但GSK也有可能继续享受没有仿制药竞争的市场。而该公司也已做好最坏的打算,即今年可能失去舒利迭在美国市场一半的销售额,英国市场销售额将下降至7.5亿英镑(合10.6亿美元),全球销售额预计将减少25%。
5、Xolair:尚无生物类似药申请上市
[专利到期时间] 2018年
2003年,罗氏和诺华(Novartis)联合研发的Xolair首次获批。该药为罗氏带来了非常可观的收入来源,销量很快达到重磅炸弹药级别,诺华方面也有相近的销售收入。
该药关键专利在2018年到期,但何时将遭遇生物类似药竞争尚不明确。根据Generics and Biosimilars Initiative杂志提供的信息,Glenmark和Sorrento正在研发相关生物类似药,但都尚未向FDA提出上市申请。
Glenmark公司去年获得FDA的批准开始进行人体试验。Sorrento的临床试验合作伙伴MabTech于2016年在中国完成了临床Ⅱ、Ⅲ期研究,但其尚未对外透露在美上市的相关计划。
诺华在去年年报中指出,Xolair的复合专利将于2018年到期,而其他的注射配方专利将分别于2021、2024年到期。同时,诺华正在对该药进行用于治疗鼻息肉的Ⅲ期临床试验,该适应症可能在2020年向FDA提交补充申请。
6、Epogen/Procrit:迎来辉瑞竞争
[生物类似药预计上市时间] 2018年
重组人红细胞生成素的生物类似药在欧洲已上市十多年,而美国市场进度严重滞后。该药的商品名为Epogen(由安进推出)或Procrit(由强生推出),用于治疗由慢性肾病或治疗引起的贫血症。去年,该药在美国的销售额达到17.7亿美元。
强生表示早已做好2018年美国市场将正面受到生物类似药竞争的准备。据安进透露,Epogen已在2013年和2015年失去一些专利保护。
FDA于2017年6月向辉瑞的生物类似药Retacrit的申请发出一份完整回复函,提到制造工厂未达标的情况,但并未要求新的数据支持。事实上,2015年FDA曾拒绝该药的申请,要求提供更多临床数据,该药的上市也因此延迟了几年。辉瑞的优势在于,FDA认为该药与安进的原研药Epogen几乎相同,且有专家委员会建议批准。辉瑞在2017年11月重新向FDA提交申请,并于近日通过了审批。辉瑞表示,Retacrit上市时间受多种因素影响,但公司在为年内上市计划作准备。
此外,山德士也已完成了Ⅲ期试验,并在欧洲推出了Epogen的生物类似药。据透露,山德士正在调整升级对该药在美国的申请策略。
7、Restasis:未如愿围堵仿制药
[仿制药预计上市时间] 2018年4-7月
去年,艾尔建(Allergan)为保护Restasis免受专利挑战,而将专利转让给美国一个原住民部落“圣瑞吉斯莫霍克部落”,该部落又将专利独家回授予艾尔建,这一举动引来媒体的广泛关注。但在10月,由于美国德州东区联邦法院判决其对梯瓦等一众仿制药企专利侵权的起诉无效,该公司还是将正面遭遇仿制药的竞争。
艾尔建曾对此策略进行了辩护,其对美国整个知识产权保护体系提出质疑,认为美国专利与商标局(PTO)的专利审判和上诉委员会除了解决联邦法院常见的专利纠纷之外,对专利保护有限。该公司呼吁美国国会介入改革。
对于艾尔建来说,法院的决定会令其很受伤。Restasis是该公司最畅销的产品之一, 2017年该药的美国销售额为14.1亿美元。在该公司2017年第四季度电话会议上,艾尔建前首席财务官Maria Teresa Hilado预测仿制药可能在2018年4-7月上市。
伯恩斯坦(Bernstein)分析师Ronny Gal及其团队同样预测该药今年将遭遇仿仿制药竞争,面临50%的收入损失。当前,FDA一直在加速仿制药审批程序。
8、Cialis:销售额恐大幅下滑
[专利到期时间] 2018年9月27日
去年,Cialis就出现在FiercePharma的畅销药专利悬崖名单中。但在7月,礼来(Eli Lilly)与多家仿制药生产商达成和解协议,成功地延长了几个月的市场独占期。
该药的主要专利已于去年11月到期,礼来目前还能使用2020年到期的单位剂量专利来抵御仿制药竞争。不过,仿制药企仍有权利在今年9月开始销售他们的产品。
礼来总法律顾问Michael Harrington透露,2020年之前,礼来的专利是“有效却被侵犯的”,礼来与一众仿制药企达成的交易包括一项“权利金许可协议”,可为该公司带来更多的确定性。
在2003年首次获得批准后,Cialis在市场上有了很大的发展。过去几年,礼来通过大量广告宣传建立了自己的品牌形象。
辉瑞的抗ED产品西地那非(Viagra)已遭受激烈的仿制药竞争,在该药迎来仿制药竞争的第四个季度,Cialis的销售额也下滑了12%,至5.97亿美元。
分析师此前预测,Cialis也将在未来几年面临急剧下滑,到2022年,其销售额将减少至5500万美元。梯瓦、太阳制药和Aurobindo的仿制药已获得FDA的暂时性批准。
9、Sensipar:仿制药整装待发
[专利到期时间] 2018年3月8日
安进的Sensipar同样是很难被仿制的一只原研药,该药的主要专利于今年3月8日到期,但其还拥有一个2026年到期的配方专利,安进正在基于该专利为Sensipar的仿制药竞争作充分防御准备。
安进还为赢取该药的儿童药市场独占权与FDA展开了法律方面的交锋。此前,FDA拒绝了安进对6个月额外的市场独占权的申请。该公司随后发起诉讼称,FDA对Sensipar的儿童药排他性的界定不同于其对强生产品的做法。今年2月,安进败诉,该案件引起了广泛关注。
几周后,FDA批准了Cipla和Aurobindo公司的仿制药,这两只仿制药何时上市仍不得而知。
分析师Ronny Gal称,安进目前已解决了与多家仿制药企的专利纠纷。2018年下半年之前与安进达成和解的公司将在2018下半年到2019年年底间上市相关仿制药产品。
安进的2018年销售预期存在十亿美元的浮动空间,该公司高管将其归因于Sensipar销量预期的较高不确定性。分析师认为,今年Sensipar的收入会有所下降,全球销售额预计将降至13亿美元,低于2017年的17亿美元。
10、Zytiga:专利期争议暂落下风
[仿制药预计上市时间] 2018年10月
强生认为其抗前列腺癌重磅药Zytiga今年不会迎来仿制药竞争,而瑞士信贷(Credit Suisse)分析师Vamil Divan则预测该药将在今年遭遇仿制药竞争。
今年1月,强生在美国专利审判和上诉委员会(PTAB)处遇挫。当时,Argentum制药公司对Zytiga的2027年专利期限申请提出上诉,最终强生在多方审查中败下阵来。因此,Zytiga专利期限仅到2018年。强生表示,其将要求PTAB进行重审,或对PTAB打击其专利权的行为提起上诉。
据瑞士信贷预计,今年Zytiga的销售额将稳定在24亿美元。此后到2026年之间,其将迎来很长一段销量下滑期,年销售额可能降至4600万美元。
关键词:
|